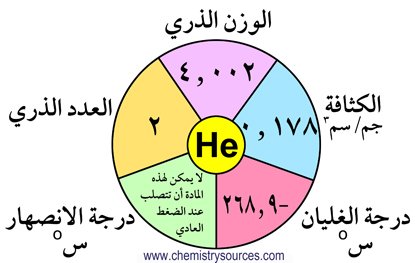
هيليوم Helium: عنصر كيميائي خامل عديم اللون و عديم الرائحة يقع في المجموعة الثامنة عشرة من الجدول الدوري و عدده الذري 2 ، أما وزنه الذري فهو 4.0026 و.ك.ذ ، و رمزه He اشتق اسمه من الكلمة اليونانية Helois و معناها الشمس . في عام 1868 
 اكتشف الفلكي الفرنسي بيير جانسين الهليلوم في طيف هالة الشمس خلال عملية كسوف الشمس و في وقت لاحق تم التعرف عليه كعنصر جديد و تم اطلاق عليه هذا الاسم من قبل الكيميائي البريطاني السير إدوارد فرانكلين و الفلكي البريطاني السير جوزيف نورمان لوكير . تم أستخلاص الغاز أول مرة من مصادره الارضية من قبل الكيميائي البريطاني السير ويليام رامزي عام 1895 و الذي اكتشفه في معدن الكليفايت . و في عام 1907 بين الفيزيائي البريطاني السير أرنيست رذرفورد بأن جسيمات ألفا هي انوية ذرات الهيليوم و التي تم التأكد من ذلك لاحقا . الهيليوم عنصر احادي الذرة و يعتبر من اخف الغازات بعد الهيدروجين. و الهيليوم مثله مثل باقي العناصر النبيلة أو الخامله فهو خامل كيميائيا و مداره الوحيد ممتليء بالالكترونات مما يصعب عليه التفاعل مع اي عناصر اخرى كيميائيا و ان حدث تكون المركبات الناتجة غير مستقرة . يعتبر الهيليوم من اصعب الغازات تسييلا و من المستحيل تجميده عند الضغط الجوي العادي و هذه الخصاصئص جعلت سائل الهيليوم من اهم السوائل المستخدمة للتبريد حيث ان درجة حرارة سائل الهيليوم تقارب الصفر المطلق و يمكن تبريد سائل الهيليوم إلى الصفر المطلق تقريبا عند الضغط الجوي العادي من خلال الازالة السريعة للبخار الموجود فوق السائل . و عند درجة حرارة فوق الصفر المطلق تقريبا فإنه يتحول إلى الهيليوم II أو الهيليوم السائل الأمثل ( الموائع العليا أو الخففيفة ) و هو سائل ذو مواصفات فيزيائية خاصة و فريدة ، فهو ليس له درجة تجمد و لزوجته تقريبا صفرا و هو يستطيع المرور بسهولة في الفتحات و التشققات الصغيرة لدرجة انه يمكن ايضا ان ينسل من فتحة العبوة الحاوية له المحكمة الاغلاق .
اكتشف الفلكي الفرنسي بيير جانسين الهليلوم في طيف هالة الشمس خلال عملية كسوف الشمس و في وقت لاحق تم التعرف عليه كعنصر جديد و تم اطلاق عليه هذا الاسم من قبل الكيميائي البريطاني السير إدوارد فرانكلين و الفلكي البريطاني السير جوزيف نورمان لوكير . تم أستخلاص الغاز أول مرة من مصادره الارضية من قبل الكيميائي البريطاني السير ويليام رامزي عام 1895 و الذي اكتشفه في معدن الكليفايت . و في عام 1907 بين الفيزيائي البريطاني السير أرنيست رذرفورد بأن جسيمات ألفا هي انوية ذرات الهيليوم و التي تم التأكد من ذلك لاحقا . الهيليوم عنصر احادي الذرة و يعتبر من اخف الغازات بعد الهيدروجين. و الهيليوم مثله مثل باقي العناصر النبيلة أو الخامله فهو خامل كيميائيا و مداره الوحيد ممتليء بالالكترونات مما يصعب عليه التفاعل مع اي عناصر اخرى كيميائيا و ان حدث تكون المركبات الناتجة غير مستقرة . يعتبر الهيليوم من اصعب الغازات تسييلا و من المستحيل تجميده عند الضغط الجوي العادي و هذه الخصاصئص جعلت سائل الهيليوم من اهم السوائل المستخدمة للتبريد حيث ان درجة حرارة سائل الهيليوم تقارب الصفر المطلق و يمكن تبريد سائل الهيليوم إلى الصفر المطلق تقريبا عند الضغط الجوي العادي من خلال الازالة السريعة للبخار الموجود فوق السائل . و عند درجة حرارة فوق الصفر المطلق تقريبا فإنه يتحول إلى الهيليوم II أو الهيليوم السائل الأمثل ( الموائع العليا أو الخففيفة ) و هو سائل ذو مواصفات فيزيائية خاصة و فريدة ، فهو ليس له درجة تجمد و لزوجته تقريبا صفرا و هو يستطيع المرور بسهولة في الفتحات و التشققات الصغيرة لدرجة انه يمكن ايضا ان ينسل من فتحة العبوة الحاوية له المحكمة الاغلاق .
و الهيليوم يعتبر ثاني اكثر العناصر وجودا في الكون بعد الهيدروجين و على الرغم من ذلك يعتبر نادرا الوجود في الارض فهو يوجد مع الغاز الطبيعي محتجزا في الجيوب الموجودة تحت سطح الارض ، و فور تحرر تلك الغازات فإن الهيليوم و نظرا لخفته فإنه ينطلق نحو الغلاف الغازي و بالتالي يصعب استرجاعه . يوجد الهيليوم فوق مستوى سطح البحر و عند الضغط الجوي الطبيعي بنسبة 5.4 جزء في المليون و هذه النسبة تزداد قليلا عند الأنتقال للأعلى . و يحتوي جزء واحد من هيليوم الغلاف الجوي على نظير الهيليوم 3 المشع و الذي يعتقد بأنه ناتج عن تحلل التريتيوم . أما نظير الهليوم 4 فإنه يعتقد بأنه ناتج عن التحلل الإشعاعي للصخور عن طرق اشعاع جسيمات ألفا .
للهيليوم عدة استخدامات فهول حل محل الهيدروجين في تعبئة المناطيد لكونه غير قابل للإشتعال ، كما يدخل الهيليوم في وقود الصواريخ ، كما يدخل الهيليوم في صناعات المفاعلات النووية كوسط نقل حراري ، كما أن الهيليوم حل محل النيتروجين في صناعات أسطوانات التنفس المستخدمة من قبل الغواصين . و نظرا لخطورة الهيليوم فأنه يعبأ في اسطوانات خاصة من الفولاذ محكمة الإغلاق بكميات قليلة و في حالة تعبئته بكميات كبيرة تضع الأسطوانات في حاويا خاصة معدة لتلك الغاية .
بوسترات (لوحات) كيميائية بدقة عالية (أكثر من 25 لوحة) من تصميم الأستاذ أكرم أمير العلي
تطبيقات كيميائية من تصميم الأستاذ أكرم امير العلي متوفر للجوالات التي تعمل بنظام أندرويد android على سوق جوجل بلاي google play
1 – تطبيق ملصقات الجدول الدوري باللغة العربية : بطاقات تحتوي على معلومات شاملة و مختصرة في نفس الوقت كل عنصر على حدة (اللغة العربية).
https://play.google.com/store/apps/details?id=com.akramir2
2 – تطبيق ملصقات كيميائية: ملصقات بتصميم جميل جدا للكواشف و الأدلة و الزجاجيات المستخدمة في المختبر و كذلك ملصقات و بطاقات لخزانات حفظ المواد و الأدوات الزجاجية .
https://play.google.com/store/apps/details?id=com.akramir
3 – إذا كنت تواجه صعوبة في تحضير المحاليل الكيميائية الأكثر شيوعا في مختبرات الكيمياء و الاحياء، فهذا التطبيق سوف يساعدك كثيرا في تحضير المحاليل :
مقالات قد تفيدك :
 مصادر الكيمياء موقع لتعليم الكيمياء بصورة مبسطة
مصادر الكيمياء موقع لتعليم الكيمياء بصورة مبسطة