كهروسالبية electronegativity :
تعرف الكهرسلبية بانها قدرة الذرة على جذب الإلكترونات التي تربطها بذرة أخرى في الجزيء و هي نصف حاصل جمع قيم الألفة الإلكترونية و طاقات التأين : و يمكن حسابها من خلال العلاقة التالية :
EA = ( IE + EA ) /2
حيث IE طاقة التأين و EA الألفة الإلكترونية و EA الكهرسلبية .
و يقال عن العغنصر الذي يميل إلى اكتساب إلكترون بأنها كهرسالب بينما يسمى العنصر الذي يميل إلى فقد إلكترون بأنه كهرموجب . إن اول من حاول حساب الكهرسلبية هو العالم ميليكان و الذي اقترح بأنه الكهرسلبية تنناسب مع الوسط الحسابي لطاقة تالتأين و الألفة الإلكترونية و لسبب عدم توفر قيم الألفة الإلكترونية لعدد من العناصر فإن تلك الطريقة وجدت صعوبة في تطبيقها على عدد من العناصر .
و في عام 1930 تمكن العالم لينس بولينج من معرفة الكهرسلبية لذرات العناصر مستخدما طريقة تقوم على حساب الفرق بين طاقات تفكك الروابط للجزيئات ثنائية الذرة ، و تعرف طاقة تفكك الرابطة بأنها الطاقة اللازمة لكسر الرابطة في مول واحد من جزيء ثنائي الذرة .
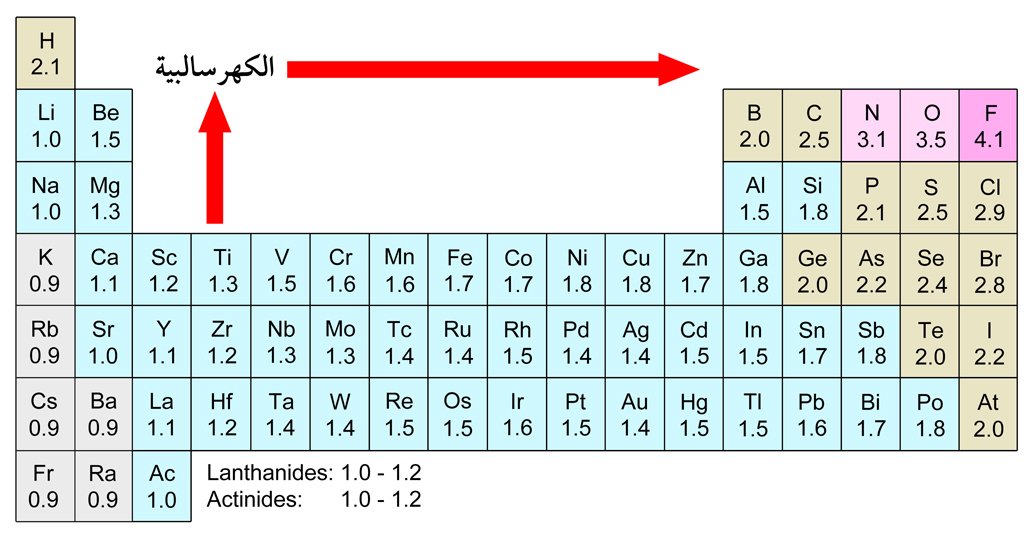
تدرج الكهروسالبية في الجدول الدوري
و عند دراسة الكهرسلبية يلاحظ ما يلي :
1 – في المجموعة الواحدة تقل الكهرسلبية من اعلى لأسفل و هناك عدم انتظام لقيم الكهرسلبية للعناصر الإنتقالية .
2 – في الدورة الواحدة تزداد الكهرسلبية من اليسار إلى اليمين و ايضا عدم انتظام لقيم الكهرسلبية للعناصر الإنتقالية .
3 – قيم الكهرسلبية لعناصر الأكسجين و النيتروجين و الكبريت و الهالوجينات تكون أعلى ما يمكن .
4 – قيم الكهرسلبية للعناصر القلوزية و القلوية الترابية تكون ادنى ما يمكن .
5 – العناصر النبيلة ليس لها كهرسلبية .
بوسترات (لوحات) كيميائية بدقة عالية (أكثر من 25 لوحة) من تصميم الأستاذ أكرم أمير العلي
تطبيقات كيميائية من تصميم الأستاذ أكرم امير العلي متوفر للجوالات التي تعمل بنظام أندرويد android على سوق جوجل بلاي google play
1 – تطبيق ملصقات الجدول الدوري باللغة العربية : بطاقات تحتوي على معلومات شاملة و مختصرة في نفس الوقت كل عنصر على حدة (اللغة العربية).
https://play.google.com/store/apps/details?id=com.akramir2
2 – تطبيق ملصقات كيميائية: ملصقات بتصميم جميل جدا للكواشف و الأدلة و الزجاجيات المستخدمة في المختبر و كذلك ملصقات و بطاقات لخزانات حفظ المواد و الأدوات الزجاجية .
https://play.google.com/store/apps/details?id=com.akramir
3 – إذا كنت تواجه صعوبة في تحضير المحاليل الكيميائية الأكثر شيوعا في مختبرات الكيمياء و الاحياء، فهذا التطبيق سوف يساعدك كثيرا في تحضير المحاليل :
مقالات قد تفيدك :
 مصادر الكيمياء موقع لتعليم الكيمياء بصورة مبسطة
مصادر الكيمياء موقع لتعليم الكيمياء بصورة مبسطة